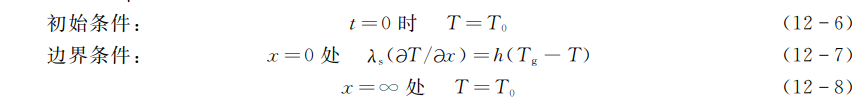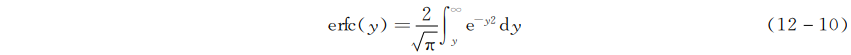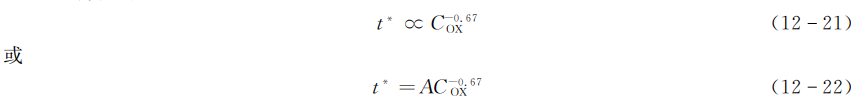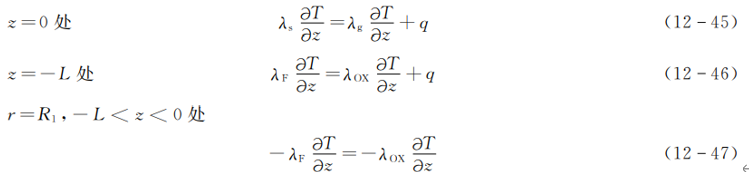第12章发动机内点火与熄火
本章介绍固体火箭发动机点火过程、点火理论和常用熄火方法。
12.1点火过程与点火理论
12.1.1点火过程
固体火箭发动机点火器工作后,点火过程就开始,如图12-1所示。
发动机的点火过程一般分3个阶段:
(1)推进剂点火阶段AB。点火燃气对推进剂表面加热,局部点燃。
(2)火焰传播阶段BD局部点燃后,火焰迅速传播到整个燃烧表面。 (3)压力建立阶段DE。燃烧表面点燃后,燃烧产物充填燃烧室,使压力迅速升高,直至建立稳定燃烧的平衡压力。 从点火器开始工作到建立稳定燃烧室压力这一点过程所经历的时间,称为发动机的点火延迟期。通常这个时间为数毫秒至数百毫秒。其中推进剂点燃阶段AB所对应的时间称为推进剂的点火延迟期,约为数毫秒到数十毫秒。这一时间虽不长,但是这一阶段工作的好坏对推进剂能否顺利地过渡到稳态燃烧、完成整个点火过程却起着关键作用。因此,对点火过程的研究,主要集中于对推进剂点火的研究。
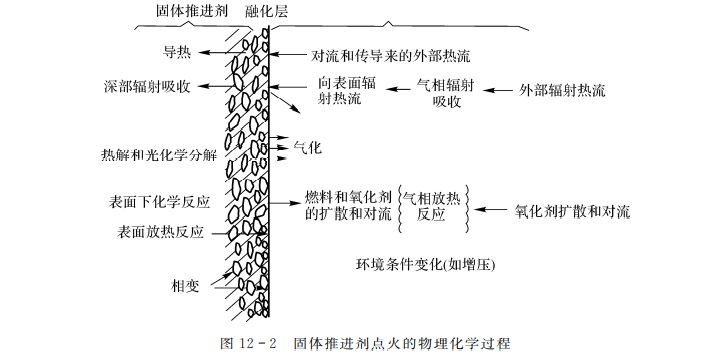
固体推进剂点火是一个复杂的物理化学过程,如图12-2所示。点火开始时,必须通过外加能量激励作为初始动力。这种激励可分3类:一是热能激励,二是化学能激励,三是机械能激励。当上述一种或数种能量激励作用于推进剂时,一系列物理化学过程就相继发生。先是经过一段时间的惰性加热,在推进剂表面上形成一个薄的融化层。接着,有的组分开始分解,根据推进剂的成分不同,分解开始的条件也不同。随后因热传导、辐射能的深部吸收和光化学分解,表面下的化学反应和热分解全面开始。由于加热继续进行,融化层继续气化,有的组分直接从表面升华。气化或升华产物(包括燃料和氧化剂)扩散到环境气体中去,而环境气体同时也向推进剂表面方向扩散。各组分在气相区、固相区和气固两相的交界面上可以分别或同时发生若干化学反应。气相反应是由推进剂气化而来的氧化剂与燃料之间或由推进剂气化而来的燃料与环境气体中氧成分之间的反应。界面上的复相反应是气相成分与凝相表面之间的反应。固相反应是推进剂固相区内各组分之间的化学反应。上述各种反应有些是吸热的,有些是放热的。要达到完全点燃状态,这些反应放出的热量必须大于吸收和散失的热量,前者与后者之差称为净热积累,它使各区的温度升高最终出现了以高速化学反应、高放热率并伴随有发光为特征的“突变”现象,使推进剂过渡到稳定的自持燃烧。只要“突变”现象一出现,就认为推进剂的点火完成了。
在推进剂点火过程中,各区的化学反应对总释放热所起作用的大小各有不同。人们把对点火发生过程中影响最大的化学反应称为关键性反应。由于在不同时期所研究的推进剂不同以及对关键性化学反应的认识不同,出现了各种点火理论。
1950年希克斯( Hicks)等人提出了固相点火理论,又称点火的热理论。这是最早提出的一个点火理论。该理论认为推进剂点火主要依靠固相化学反应产生的净热积累,使化学反应达到高速度、高放热率的“突变”条件。它忽略了气相和复相化学反应的作用。
在1960年,麦卡勒维( McAlevy)、科恩(Cohn)和萨默菲尔德提出了气相点火理论。在这方面除库玛(Kumar)和赫孟斯( Hermance)出的模型外,大都为一维模型。该理论认为点火的发生主要依靠气相化学反应产生的净热积累,使气相化学反应达到高速、高放热率的“突变”条件。它忽略了固相和界面上化学反应的作用。
到1963年,安德森(Anderson)等人首先提出了复相点火理论,认为推进剂气固两相交界面上的复相反应是完成点火的主要原因。室温的点火气体与推进剂表面接触后,表面上立即产生激烈的放热化学反应,促使推进剂点火,因而有时也称为自燃点火理论。
上述三种理论,都是强调了点火过程中各种化学反应的某一主要反应,对于不同类型的推进剂和不同的点火方式,这种强调可能符合实际情况,但都偏于过简,不能真实地描述复杂的点火过程。布雷德利(Bradley)库玛等人提出了一种综合点火理论。它认为各区中的反应都有重要作用,应当予以综合考虑。
在推进剂点火机理研究中,推进剂的点火延迟期是一个重要参数,它表示推进剂完成点火所需要的时间,具体讲就是从施加点火能量激励开始到推进剂表面上出现第一个火苗为止的时间。点火延迟期通常由三部分时间组成:惰性加热时间、气体对流和扩散的混合时间和化学反应时间。由于混合时间与化学反应时间之间没有明显的界线,且有一定的重叠,因此点火延迟期并不是这三部分时间的代数和。
要准确地确定点火延迟期,就要选择合适的点火准则目前在理论分析和实验研究中所应用的点火准则是多种多样的。
理论研究用的点火准则包括:
(1)推进剂表面温度\({{T}_{s}}\)大于或等于某一临界值,即\({{T}_{s}}\ge {{\left( {{T}_{s}} \right)}_{cr}}\),又称为点火的温度准则。
(2)推进剂表面温度\({{T}_{s}}\)的升高速率大于或等于某一临界值,即\(d{{T}_{s}}/dt\ge {{\left( d{{T}_{s}}/dt \right)}_{cr}}\)。
(3)推进剂表面温度\({{T}_{s}}\)随时间t的变化曲线上出现拐点,即\({{T}_{g}}\ge {{\left( {{T}_{g}} \right)}_{cr}}\)。
(4)气相区气体温度\({{T}_{s}}\)大于或等于某一临界值,即\({{T}_{g}}\ge {{\left( {{T}_{g}} \right)}_{cr}}\)。
(5)气相区火焰的发光强度J大于或等于某一临界值,即\(J\le {{J}_{cr}}\)。
(6)气相区化学反应速率\(\omega \)大于或等于某一临界值,即\(\omega \ge {{\omega }_{r}}\)。
实验研究用的点火准则包括:
(1)高速摄影机摄影时观察到的第一个火苗。
(2)光电管观察到发光强度的剧烈变化。
(3)热电偶测出热流密度或温度的突变。
点火准则是判定推进剂是否点火的标准,为使理论分析得到的点火延迟期能与实验测定的点火延迟期进行比较,必须使理论点火准则和实验点火准则一致,例如理论准则(5)和实验准则(2)就是一致的。
基于对点火过程的理论分析和实验测定,将各种参数对点火延迟期的影响综述如下:
(1)外部加热热流密度q越高,点火延迟期越短。在惰性加热期间点火延迟期与加热热流密度的二次方成反比。
(2)点火压力增大,点火延迟期缩短。当点火压力很高时,点火延迟期与压力的相关性降低。
(3)环境气体含氧量增加,点火延迟期缩短。
(4)点火气体与推进剂的热响应比√(cp)(c)增大时,点火延迟期增加
(5)点火压力的增压率增加时,点火延迟期缩短。
(6)初始温度(包括点火气体和推进剂)越高,点火延迟期越短。
(7)点火气体的流速及共热粒子的冲击速度高时,点火延迟期短。
(8)推进剂表面粗糙度大时,点火延迟期短。
(9)推进剂的组成及各组分所占比例的大小、粒度大小,对点火延迟期都有较大的影响。
12.1.2固相点火理论
由希克斯首先建立的固相点火理论认为固体推进剂点火是外加热能激励和由此而产生的凝相放热化学反应二者共同作用的结果。作如下假定:
(1)固体推进剂是化学活性物质。
(2)点火期间没有质量扩散和表面退移。
(3)环境气体中含氧量等对点火过程没有影响。
(4)热传导是半无限一维模型。
其控制方程为
式中\({{\rho }_{\text{p}}}\),\({{C}_{s}}\)和\({{\lambda }_{s}}\)分别表示推进剂的密度、热和导热系数;E和Q分别表示推进剂的活化能和单位质量反应热;Z为指前因子。若\({{T}_{g}}\)为点火气体温度,其边界条件为
x=0时 \(-{{\lambda }_{s}}(\partial T/\partial x)=h({{T}_{g}}-T)\)
x=∞时 \(T={{T}_{0}}\)
在该理论中,点火气体的温度T是变化的,从t=0到t=t0期间点火气体的温度为Tg1,当t>t0时,点火气体温度下降,或停止加热,T变为T而T>T2,因而其初始条件为
0<t≤t时 \({{T}_{g}}={{T}_{g1}}\)
t>to时 \({{T}_{g}}={{T}_{g2}}\)
t=0时 \(T={{T}_{0}}\)
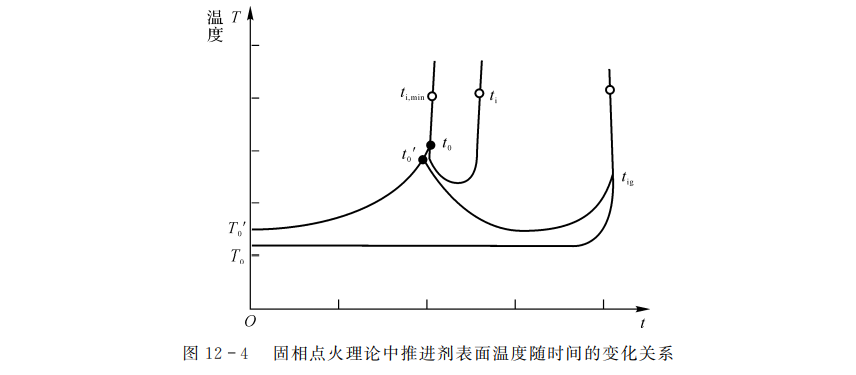
式(12-1)不能求得解析解,希克斯在一定范围内进行了数值计算,其结果表示在图12-4中,为推进剂表面温度T随时间t的变化曲线。
由图可知,当推进剂受到温度为T1的热气体作用时,存在着一个最小点火延迟期\({{t}_{i,mim}}\)。此时,一方面因传热使推进剂表面及表面内的固相区温度升高,另一方面因方程式(12-1)中反应热项\(\rho QZ\exp (-E/{{R}^{0}}T)\)的存在,进一步升高了表面内固相区的温度。随着温度的提高,反应热项的作用更加增强。这样,在连续加热和反应热项连续作用的条件下,推进剂表面温度就会在短时间内达到点火条件希克斯把这种点火时间称为最小点火延迟期\({{t}_{i,mim}}\)。根据计算,他认为表面温度T=0.045(E/R0)时,就算点着火了。这是希克斯研究的第一种点火情况。
希克斯研究的第二种点火情况是绝热点火过程因推进剂是化学活性物质,有化学反应热项作自加热热源在无外加热热源作用和绝热条件下,经过足够长时间,推进剂就可达到点火条件。他把这种情况下的点火时间称为绝热点火延迟期tat的大小与推进剂的初始温度T有关。T越大t就越小实际上,由于推进剂尺寸有限,表面上总会有一定的热损失,因而当T。低于某一临界值时,就不可能达到点火条件。
第三种点火情况是用点火气体温度为\({{T}_{g1}}\)的热源加热,当\(t={{t}_{0}}={{t}_{i,min}}\)时停止加热,使环境温度下降到\({{T}_{g2}}\),这时推进剂表面温度就会下降。可是由于固相中的放热化学反应的作用,当生成热大于损失热时,表面及表面内的固相区的温度就会升高。一般讲,经过一段时间\({{t}_{i}}({{t}_{i}}{{>}_{ti,min}})\),但\({{t}_{i}}<<{{t}_{i,a}})\)后,就可达到点火条件。当用温度为\({{T}_{g1}}\)的气体加热时间\({{t}_{0}}\)减小时,点火延迟期\({{t}_{i}}\)就会变大。当\({{t}_{0}}\to 0\)时,\({{t}_{i}}\to {{t}_{ia}}\)
希克斯的固相点火理论对双基推进剂的点火过程提供了一个比较满意的分析方法。但因为忽略了气相过程的作用,所以要用它解释复合推进剂的点火过程是有困难的。
为了简化分析过程,在强迫对流加热的点火条件下固相反应生成热对点火过程影响较小时,就可将式(12-1)中的反应热项忽略不计这时式(12-1)就变成
式中,\({{a}_{s}}={{\lambda }_{s}}/\rho P{{C}_{s}}\),是推进剂的热扩散率。
其解析解为
式(12-9)表达了推进剂内部温度T随x和t的变化关系。式中余误差函数的定义为
在式(12-9)中余误差函数的自变量有两个分别为\({{y}_{1}}=x/2\sqrt{{{a}_{s}}t};{{y}_{2}}=x+h\sqrt{{{a}_{s}}t}/{{\lambda }_{s}}\)。
点火过程中,推进剂表面温度最高,根据点火的温度准则,只要表面温度达到点火温度\({{T}_{ig}}\)时,即可着火燃烧。由式(12-9)可知,当x=0时,就可导出推进剂表面温度T随时间t变化的关系式
由式(12-11)可知,\({{T}_{s}}\)随t的增加而升高,并且以\({{T}_{g}}\)为极限。这表明,只要点火气体温度\({{T}_{g}}\)超过推进剂点火温度\({{T}_{ig}}\),终究是会发生点火的。令\({{T}_{s}}\)=\({{T}_{ig}}\),且当\(h\sqrt{{{a}_{s}}{{t}_{i}}}\ll 1\) 时,就求得点火延迟期\({{t}_{i}}\)为
式(12-12)表明,推进剂的\(\lambda {{\rho }_{p}}{{c}_{s}}\)越小,点火温度\({{T}_{ig}}\)越低,初始温度To越高,点火气体温度\({{T}_{g}}\)和对流换热系数h增大时,点火延迟期\({{t}_{i}}\)就缩短。
12.1.3气相点火理论
固相点火理论不能解释复合推进剂的点火过程。麦卡勒维等人利用激波管研究片形燃料试件在氧化性气体中点火的现象,提出了气相点火理论。该理论认为,点火热气体是氧化性气体,它加热推进剂并使燃料成分分解、气化为气体产物,与点火气体相互扩散、混合。由于点火气体的加热和气相放热反应的作用,导致气相区发生点火。气相点火理论模型的物理化学过程如图12-5所示。其假设如下:
(1)燃料试件以不变的速率分解和气化。
(2)燃料试件表面温度是由两个半无限大物体表或燃料扩散化学反应和放热面接触时的热传导问题的解来求得的
(3)点火气体成分在点火过程中保持不变。
(4)气相的压力保持均匀一致。
(5)气相反应为二级反应。
(6)气相对固相的热交换方式为热传导,且气相的温度分布不受扩散过程的影响。
(7)固相的反应或分解不产生热效应。
(8)从气相发生“突变”反应到出现火苗之间的时间极短,可以略去不计。点火延迟期就是燃料分解、气化、扩散并与氧成分混合达到“突变”反应的时间。
(9)对一般复合推进剂,当温度在600K以下时,燃料比过氯酸铵气化得更快,因而推进剂表面是燃料气体的唯一来源。过氯酸铵和铝粉可看作一种惰性物质
控制方程如下:
扩散方程:
能量方程:
初始条件:
t=0时
边界条件:
式中,表示化学当量计算比;\(C_{OX}^{0}\)表示氧化剂初始浓度;Q为反应热。下角标OX和F分别表示氧化剂和燃料。
根据初始条件式(12-16)和边界条件式(12-7)、式(12-18)对方程式(12-13)求解,可知氧化剂浓度Cox不随时间地点变化,其数值等于初始值,即
\({{C}_{OX}}=C_{OX}^{0}\) (12-19)
对方程式(12-14)求解,可得出燃料的浓度变化规律为
式中,m为燃料质量生成率,根据假设是一个常量。
将式(12-19)和式(12-20)代入式(12-15),经过简化并计算后可知,当\(t={{t}^{*}}\),在\(x={{x}^{*}}\)处,\(\partial T/\partial t\)由负值变到正值。从能量观点讲,这表明气相区化学反应的放热量等于损失热量就在\(\partial T/\partial t\)=0时达到。在此之后,生成热就大于损失的热量,出现了热量积累的情况。由于气相反应热项式(12-15)右边第二项的存在气相区的温度就会很快达到发火点。因此气相理论认为\(\partial T/\partial t\)=0就是“突变”反应的开始。因而\({{t}^{*}}\)就是点火延迟期\({{t}_{i}}\), \(x={{x}^{*}}\)处就是点火发生地。由计算可知
式中系数A是依赖于试件性质和试验条件的常数。该式证明点火延迟期\({{t}^{*}}\)与氧化剂浓度Cox的-2/3次方成正比,因而氧化剂浓度越大点火延迟期就越短。这进一步阐明了点火气体的组分对点火过程有较大的影响。
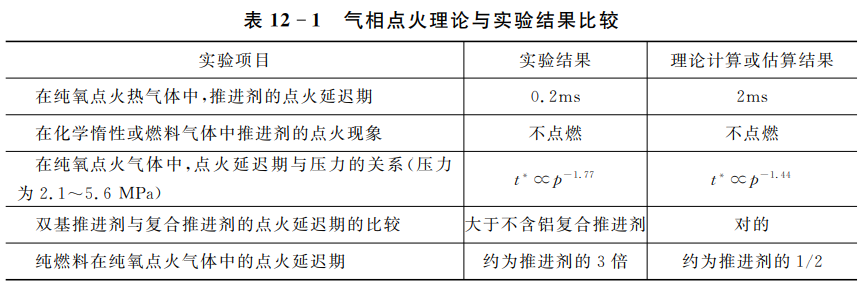
用气相点火理论曾对聚酯-苯乙烯(22%)过氧酸铵(78%)复合推进剂进行了理论计算,其计算结果与实验结果的对比见表12-1。
由表12-1可以看出,从定量角度看,理论与实验结果差距较大,但从定性角度看,二者基本上是一致的。因此,气相理论基本上反映了复合推进剂的点火实质。用它解释复合推进剂的点火机理是合理的。
12.1.4复相点火理论
复相点火理论又称为非均相点火理论。该理论认为某些氧化性液体或气体与固体推进剂在常温下接触时,就会产生激烈的放热化学反应。反应热使推进剂表面温度升高并且点火。由于点火所需的热量是由不同相物质之间的化学反应产生的,因而称为复相点火理论。以氧化性气体为例,该理论假定:
(1)热和质量扩散到半无限大氧化性气体中去和热传导进入半无限大固体推进剂的方式都是一维的。
(2)氧化性气体与固体推进剂中燃料之间的复相反应对气体而言是一级反应,对固体推进剂则属于零级反应。
(3)气体与固体燃料之间总是处在热平衡状态。
(4)气体与固体均属各向同性物质。
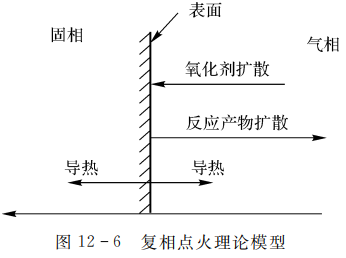
复相点火理论模型如图12-6所示。
控制方程如下:
固相热扩散方程
\(\partial T/\partial t={{a}_{s}}({{\partial }^{2}}T/\partial {{x}^{2}})\)
气相热扩散方程
\(\partial {{T}_{g}}/\partial t={{a}_{g}}({{\partial }^{2}}{{T}_{g}}/\partial {{x}^{2}})\)
氧化剂气体质量扩散方程
\(\partial {{C}_{OX}}/\partial t={{D}_{OX}}({{\partial }^{2}}{{C}_{OX}}/\partial {{x}^{2}})\)
反应产物质量扩散方程
\(\partial {{C}_{P}}/\partial t={{D}_{P}}({{\partial }^{2}}{{C}_{P}}/\partial {{x}^{2}})\)
初始条件:
当t=0时
\(T={{T}_{0}},{{T}_{g}}={{T}_{0}};{{C}_{OX}}=C_{OX}^{0};{{C}_{p}}=0\) (12-27)
边界条件:
在\(x=-\infty \)处
\({{T}_{g}}={{T}_{0}};{{C}_{OX}}=C_{OX}^{0};{{C}_{p}}=0\) (12-28)
在\(x=+\infty \)处
\(T={{T}_{0}}\) (12-29)
在x=0处
\({{T}_{g}}=T={{T}_{s}}\) (12-30)
\({{D}_{p}}(\partial {{C}_{p}}/\partial x)=\psi {{D}_{OX}}(\partial {{C}_{OX}}/\partial x)\) (12-31)
\(Q(-{{D}_{OX}})(\partial {{C}_{OX}}/{{\partial }_{x}})=-{{\lambda }_{s}}(\partial T/\partial x)+{{\lambda }_{g}}(\partial {{T}_{g}}/\partial x)\) (12-32)
\(-{{D}_{OX}}(\partial {{C}_{OX}}/{{\partial }_{x}})={{C}_{OX}}{{Z}_{\exp }}(-E/{{R}^{0}}T)\) (12-33)
式中,\({{C}_{p}}\)表示反应产物的浓度;表示反应产物与氧化剂气体之间的质量比;Q为消耗单位质量氧化剂的反应热。复相点火理论所涉及的界面条件比较复杂使用了式(12-30)~式(12-33)四个条件很明显,式(12-30)说明在交界处气相、固相和界面上的温度是相等的。式(12-31)表示扩散到界面上的氧化剂全部参加了反应,其反应产物又全部扩散到气相中去。式(12-32)表示扩散到界面上的氧化剂的反应热,一部分传导到固相区,一部分传导到气相区(这一部分热量与传导到固相区中去的热量相比很小,可以忽略不计。式(12-33)表示界面上氧化剂气体的反应速率等于它的扩散速率。
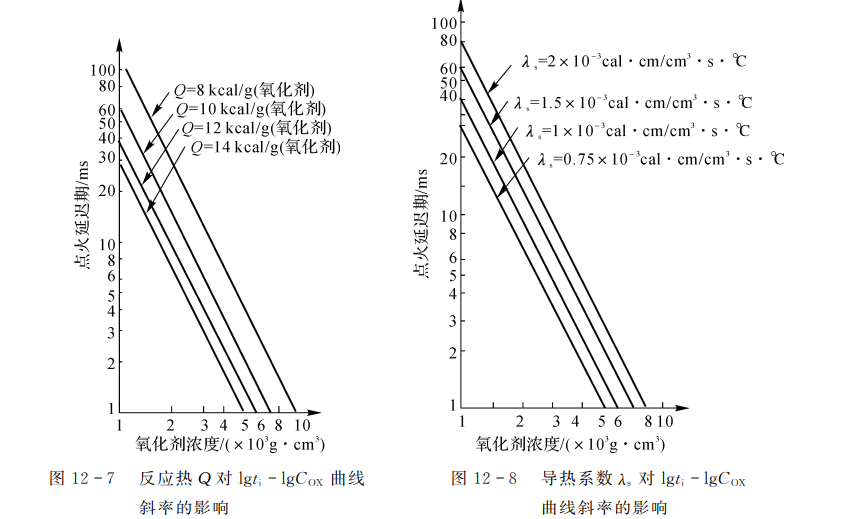
由于控制方程中存在着非线性项exp(-E/RT),因而只能用数值方法求解,其结果如图12-7和图12-8所示。它们分别表示点火延迟期t所氧化剂浓度Cox之间的关系曲线,并且反映了反应热Q及导热系数入的影响。由图可知,氧化剂浓度Co越大,反应热Q越大,导热系数入,越小,则点火延迟期越短。
复相点火理论考虑了点火环境气体对点火过程的影响,尤其是气固或液固之间的复相反应的作用,这在某一特定条件下是接近实际的,但对一般点火过程就不能反映客观实际了。
12.1.5综合点火理论
由于固体推进剂的点火过程相当复杂,发展一种综合考虑各区化学反应和传热、传质过程的点火理论即综合点火理论来代替上述各理论是十分必要的。目前,这种理论的研究还不充分,现以1980年库玛等人建立的模型为例加以说明。
提出该模型的目的是发展一个过氧酸铵复合推进剂在快速升压下点火的理论解;研究增压速率和氧化剂粒度等参数对点火过程的影响;进行实验测定,以证实这种理论的正确性。
该物理模型主要是模拟滞止区的点火情况考虑点火的物理过程是点火燃气充满燃烧室使其增压,并向推进剂传热使其表面及表面层以内温度升高,此时就出现了固相区、气相区和交界面上的各类反应。当反应放出的热量大于损失的热量时,各区的温度就会很快提高直至点火。
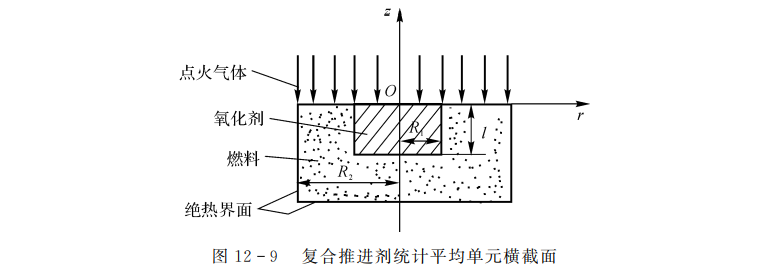
根据氧化剂粒度随机分布和氧化剂与燃料配比,取出一个统计平均单元,如图12-9所示,由氧化剂组分与燃料组分二者构成二维轴对称嵌套圆柱体。
点火燃气作用在z=0的表面上,该模型假设:
(1)遵守完全气体定律。
(2)高温分解与化学反应过程可用阿累尼乌斯公式表示。
(3)气相压力是时间的已知函数,在临近推进剂表面的一个小区域内,压力均匀相等。
(4)所有气体组分在z向和r向扩散系数相等。
(5)各组分均沿z向运动,r向的运动可忽略不计。
控制方程如下:
(1)固相区。
氧化剂中传热方程:
固体燃料中传热方程:
式中\({{q}_{F.s}}\)和\({{q}_{ox,s}}\)分别表示固体燃料和固体氧化剂单位时间单位体积中热辐射和热分解热量。
(2)气相区。
连续方程:
能量方程:
式中,\({{q}_{g}}\)表示气相单位时间单位体积内的释放热。
状态方程
式中,\(\overline{M}\) 表示平均分子量。
组分守恒方程:
式中,\({{\omega }_{j}}\(表示j组元单位时间单位体积内质量生成率;j=1,2,3,4,分别代表气态的氧化剂、\(H{{N}_{3}}HC{{O}_{4}}\) 和燃料;\({{Y}_{j}}\)表示j组分质量分数。
初始条件 当t=0时
固相区 \(T={{T}_{0}}\) (12-40)
气相区 \(T={{T}_{g}};{{v}_{z}}=0;{{Y}_{j}}={{({{Y}_{j}})}_{0}};j=1,2,3,4\) (12-41)
边界条件
(3)固相区
1) \(z=-\infty \) 处 \(T={{T}_{0}}\) (12-42)
r=0处 \(\frac{\partial T}{\partial r}=0\)
r=R2处 \(\frac{\partial T}{\partial r}=0\)
3)界面上温度连续
4)各界面热流平衡
(4)气相区。
1)在中心线与外边界上的对称条件:
r=0处
\(\frac{\partial T}{\partial r}=0;\frac{\partial {{Y}_{j}}}{\partial r}=0\) (12-48)
r=R2处
\(\frac{\partial T}{\partial r}=0;\frac{\partial {{Y}_{j}}}{\partial r}=0\) (12-49)
2) 在\(z=\infty \)
\(\frac{\partial T}{\partial z}=0;\frac{\partial {{Y}_{j}}}{\partial z}=0\) (12-50)
3)在气固交界面即z=0处,温度连续,即
\({{T}_{s}}={{T}_{g}}\) (12-51)
4)在气固交界面上质量流量平衡,即在z=0处
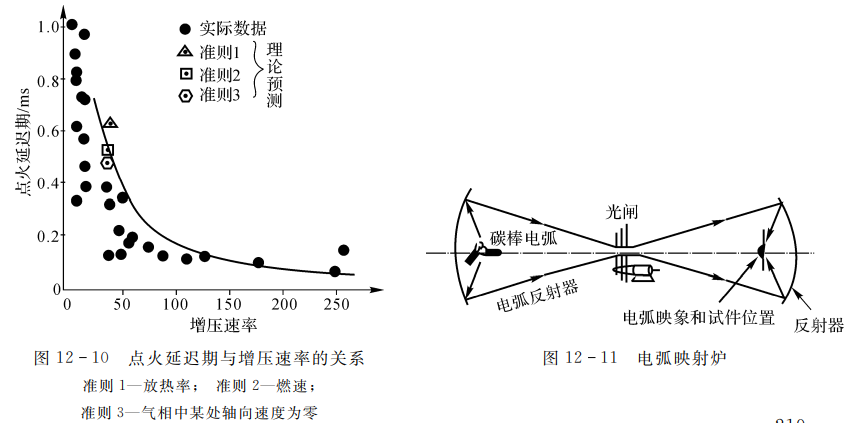
运用上述初始、边界条件,对控制方程组,式(12-34)~式(12-39)进行数值求解,可以得到点火延迟期与增压速率的关系。将理论预示结果和实验结果相对比,如图12-10所示,在定性上是一致的。
12.1.6点火实验
在点火机理研究中,实验研究是十分重要的。过去许多研究者为了证实和探讨点火过程中的机理,曾作了不少工作。米切尔( Mitchell)曾对这方面作过专门的评述,这里只作简要介绍。
按点火能量激励的类别,点火实验可分为以下6类。
(1)用冲击或摩擦方法,研究点火过程。
(2)用导热方法如用热平板、热桥丝或滞止热气体进行点火的实验研究。
(3)用辐射能如弧光映射炉中的电弧光、热辐炉中的辐射热、激光或其他光源等对推进剂进行点火的实验。
(4)用化学活性极强的氧化剂气体如过氯酸蒸气等,突然与推进剂接触的复相点火实验。
(5)用对流传热如激波风洞、固体或气体小火箭、气液式小火箭发动机产生的高温、高压、高流速燃气,对推进剂进行加热点火的实验。
(6)采用激光进行推进剂点火研究,此种实验方法,加热热流密度很大,加热时间易于控制,热流密度的大小易于精确测定,在点火实验段内可充入不同压力、不同成分的气体,以得到不同的点火环境。若在试验段设置透明窗,就可进行高速摄影,以记录点火的真实过程。利用这类装置,可以研究各种主要因素对点火过程的影响,其测量精确度高,适于研究各种理论模型。
图12-11所示的电弧映射炉就是辐射能点火的一种典型装置。
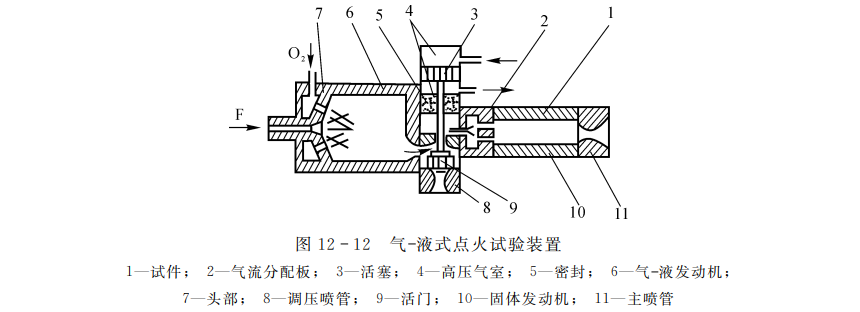
利用流动热气体点火的特点是实验条件接近发动机的实际点火过程,所测得的结果对工程设计的使用价值较高。能逼真地模拟实际点火条件,成本低廉。图12-12所示是一个气一液式小火箭发动机点火试验装置,它用的推进剂是气氧和酒精,改变其配比可获得不同含氧量和不同温度的点火气体。改变固体火箭发动机(即试验段)的喷管大小,可获得不同的点火压力。利用燃气转换机构可以获得比较理想的点火热流阶跃函数。
12.2固体火箭发动机熄火
为了扩大固体火箭发动机的应用范围,它的可控性研究日益受到重视。强迫熄火技术就是固体火箭发动机可控性研究的内容之一。从形式上看,熄火方法有降压熄火和喷阻燃剂熄火两类。
12.2.1快速降压熄火
用迅速降低燃烧室内压力的方法,可以使推进剂熄火。而快速降压的实现,是靠迅速扩大发动机排气通道截面积的方法。降压所需要的时间,一般认为与气体停留时间\({{t}_{r}}\)相等。而
式中,V为燃烧室充气容积;c为特征速度;A为排气通道截面积。
式中,k是点火燃气的绝热指数。由式(12-54)可知,扩大后的排气面积A越大,降压时间t1越小。对一定的燃烧室压力,A存在一极限值或最小值\({{\left( {{A}_{d}} \right)}_{lim}}\)只有当\({{A}_{d}}>{{\left( {{A}_{d}} \right)}_{lim}}\)时,发动机才会熄火。
1.降压熄火机理
研究证明,当压力降低时,火焰远离推进剂表面。这时气相化学反应区增厚,温度梯度变小故引起火焰对燃烧表面的传热量减小,使表面与表面层以内的热分解、蒸发和升华速度下降,这又进一步使气相化学反应速度减小,结果导致熄火。由此看来,推进剂存在一个可燃极限压力Pcr,当燃烧室内压力小于此值时,可达到熄火的目的。
降压熄火研究的内容,主要是探讨压力下降速率的临界值(dp/dt)cr它不仅与燃烧室压力有关,而且还和推进剂类型、燃烧室几何特征和喷口位置等有关。萨默菲尔德等人的实验证明,当增加推进剂中氧化剂比例或使氧化剂粒度变细时,熄火困难。增加铝粉,熄火也变难。当燃烧室压力低于2.8MPa时,增加铝粉的含量熄火变容易但效果不明显当改变黏合剂种类时,在7.0MPa压力下,聚丁二烯丙烯酸(PBAA)、端羟基聚丁二烯(CTPB)和聚氨酯(PU)都难以熄火。当压力为2.8MPa时,PBAA和CTPB推进剂的熄火性能相近,PU却更容易熄火
2.熄火条件
西普鲁赫( Ciepliuch)用压力下降50%的时间\(\Delta {{t}_{50}}\)来表征熄火参数\({{\left( {{A}_{d}} \right)}_{lim}}\)该时间与压力过渡时间 (= |dt/d(lnP))之间的关系为
实验证明,在特定条件下,对熄火存在一个压力下降时间的极大值。该极限值\(\Delta {{t}_{50}}\)对应的记为\({{\left( \Delta {{t}_{50}} \right)}_{lim}}\)。如对含81%过氯酸铵和19%聚丁二烯丙烯酸复合推进剂, \({{\left( \Delta {{t}_{50}} \right)}_{lim}}=3.5ms\)
对于压力形成时间\(\theta \( 接近气体停留时间\({{t}_{r}}\)的情况,若\({{A}_{d}}/{{A}_{t}}\),足够大(\({{A}_{t}}\)为喷管喉道截面积),环境压力Pa低于推进剂可燃极限\({{P}_{cr}}\)时,就能得到完全熄火。否则,在熄火后可能会发生再点燃。因此,保证完全熄火的条件如下:
当 \(\theta \)>tr时,就会发生缓慢熄火现象。如果Ad/At未达到(Ad/At)cr,则发动机会在新的燃烧室压力下进行稳定燃烧。
12.2.2阻燃剂熄火
向正在燃烧的推进剂表面喷射阻燃剂的熄火研究,是从发掘有效阻燃剂和喷洒阻燃剂方法两方面进行的。
1.喷水熄火
由喷水熄火的实验证明,存在一个最小喷水时间。若喷水时间小于它,就不可能熄火。不同的研究者得到了不同的最小喷水时间,而且变动范围较大,可为0.1~0.6s。其熄火延迟时间比降压熄火时间大2~4倍,所需水量\({{m}_{w}}=2M+a{{A}_{b}}\) ,式中M表示燃烧室内燃气质量,a为一经验常数。
喷水质量m和熄火延迟时间θ的大小,与喷水流率m和喷水时间t有关。法国航空和宇航研究局的实验证明,当喷水流率m足够大时,喷水时间t=1ms就可获得安全熄火当向推进剂燃烧表面喷水时,水受热蒸发吸收热量降低了表面及其附近区域的温度,使化学反应速度降低,导致燃烧室压力下降而熄火。
2.喷盐粉熄火
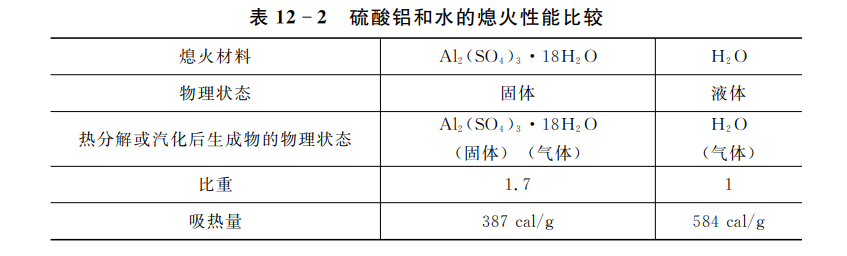
最初使用过碳酸氢铵(\(N{{H}_{4}}HC{{O}_{3}}\) )粉末用爆炸抛撒方式撒在固体推进剂表面上,其效果不佳。后来使用含结晶水的硫酸铝粉(\(A{{l}_{2}}{{\left( S{{O}_{4}} \right)}_{3}}\cdot 18{{H}_{2}}O\) )喷洒在推进剂燃烧表面上,熄火效果良好。现将各为1g质量的水和硫酸铝分解时所需要的热量列于表12-2中。
由表12-2可知,(\(A{{l}_{2}}{{\left( S{{O}_{4}} \right)}_{3}}\cdot 18{{H}_{2}}O\) )的熄火性能与水相近,这个事实已被实验所证实。盐粉喷洒在燃烧表面上时,首先将表面覆盖起来,阻碍了火焰对表面的传热,使表面温度降低,热分解、气化与升华速率减慢。其次由于盐粉的热解,吸收燃烧反应区的热量。因为隔热和吸热的作用,正常燃烧的条件遭到破坏,导致推进剂熄火。
12.2.3 快速卸压冷却熄火实验
对于某些高能推进剂,如单纯采取快速降压或阻燃剂一种措施,很难实现高能推进剂熄火,故考虑将快速降压和冷却综合起来,实现高能推进剂快速熄火。
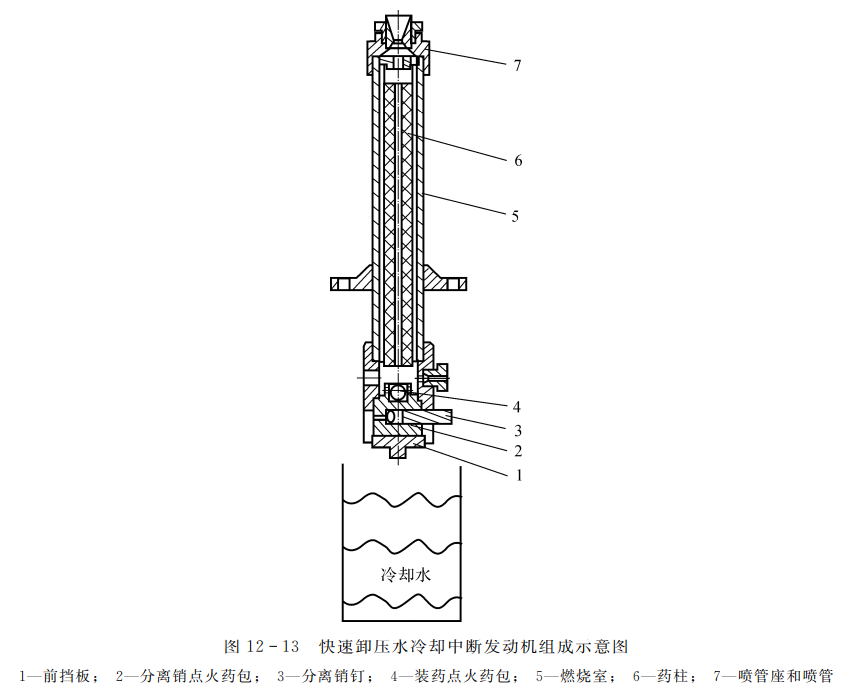
如图12-13所示,快速卸压水冷却中断发动机采用竖直放置,发动机下方为一水缸。快速卸压水冷却中断发动机工作过程如下:首先利用装药点火药包点燃推进剂药柱;药柱燃烧△t时间后,将分离销点火药包点燃,产生的燃气将分离销钉弹出;此时发动机前端打开,燃烧室压强瞬间变为大气压,同时药柱根据重力效应掉出发动机外进入水缸。由于快速卸压及水冷却,实现药柱熄火。
习 题
12.1发动机点火过程包括哪些阶段?
12.2简述固相点火理论。
12.3简述气相点火理论。
12.4简述复相点火理论。
12.5固体推进剂点火方式有哪些?
12.6火箭发动机熄火方法有哪些?
12.7分析快速降压熄火机理。
12.8对于高能推进剂,采用何种熄火方式比较有效?