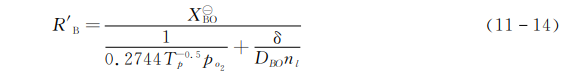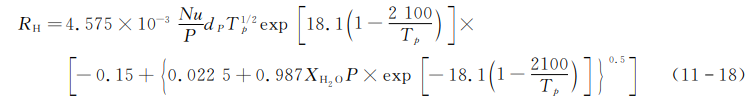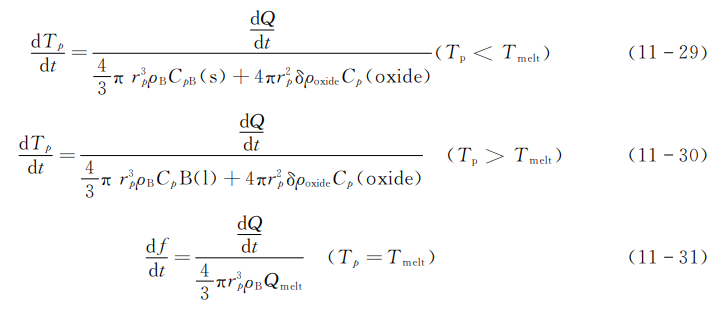第11章含金属推剂燃烧
为提高固体火箭发动机能量性能(包括质量比冲和体积比冲)和推进剂密度,常在推进剂中加入金属粉剂(如镁、铝、硼等),此外,金属及其氧化物的颗粒还能对火箭发动机工作时某些频率的声不稳定燃烧起抑制作用。
然而,和碳氢燃料相比,金属的燃烧显示出某种特异的行为,和推进剂其他组分很不一样。 例如:金属颗粒会在燃面处结团,降低燃烧效率;金属氧化物在喷管中流动时的两相流损失,使得推力效率大幅度下降;旋转发动机中的加速度场效应使结团现象更趋严重,导致燃烧特性和内弹道性能的重大变化;但是,有时候,加金属粉剂又能改善推进剂的点火与燃烧特性;这些具体效果取决于加入的金属与推进剂的性质。
上述种种现象均与推进剂中添加的金属有关,因此研究推进剂燃烧环境中金属颗粒的燃烧具有重要意义。
11.1加入金属燃料的意义及金属组分的燃烧特点
11.1.1加入金属燃料的意义
1.增加比冲(单位:N·s/kg)
一些典型固体推进剂比冲如下:
双基推进剂比冲(不含金属): 2100~2300
复合推进剂比冲(含铝镁10%~20%): 2500~2900
中能富燃料推进剂比冲(含铝镁40%): 6000~8000
高能富燃料推进剂比冲(含硼40%): 10000~12000
燃料比冲(含硼70%): 16000~20000
2.增加密度(单位:g/cm3)
一些典型固体推进剂密度如下:
双基(改性双基)推进剂密度: 1.57~1.65
含铝复合推进剂密度: 1.60~1.78
含硼复合推进剂密度: 1.55~1.70
3.抑制高频振荡燃烧
不稳定燃烧是固体火箭发动机的一种不正常工作状态,一般体现为燃烧室出现一定频率的压强震荡,压强曲线就像正弦曲线。如果压强振荡发展到一定水平,发动机会产生强烈的振动,会带来许多不良后果,如发动机部件过热,压强过高等。
为降低或防止发动机内不稳定燃烧,有许多方法目前应用比较广泛的就是利用“微粒阻尼”效果,其原理是:如果燃烧产物中含有凝相微粒,可以产生阻尼作用,使声振衰减。含铝推进剂能有效地防止高频不稳定燃烧,就是因为它燃烧生成了\(A{{l}_{2}}{{O}_{3}}\)凝相微粒,当然,其他凝相微粒也可有阻尼作用。凝相微粒能产生阻尼原因是:凝相与气相声振之间存在速度滞后和温度滞后,由于黏性和传热,产生声能损失,主要是黏性损失。阻尼效果关键在于微粒尺寸,频率越低,要求颗粒尺寸越大。\(A{{l}_{2}}{{O}_{3}}\)一般有两级配:$\text{2}\mu $和$\text{50}\mu $。
一定直径的铝微粒能产生最大阻尼的频率是一定的,两者一般有如下关系:
\({{f}_{\max }}=\frac{9\mu }{2\pi {{d}^{2}}{{\rho }_{s}}}\)
式中 \({{f}_{\max }}\)—微粒能起最大阻尼作用的频率;
\(\mu \)—燃气的黏性系数;
d—微粒直径;
\({{\rho }_{s}}\)—微粒密度。
4.不利因素
在复合推进剂中加入金属粉,主要有如下弊端:
(1)高燃烧温度,不利热防护。
(2)二相流损失,约占喷管损失的30%。
(3)引起喷喉沉积或者冲刷。
(4)高金属含量推进剂低压下燃烧效率低。
(5)产生烟尘。
(6)红外特征明显。
11.1.2金属组分的燃烧特点
1.金属及其氧化物属性
常见金属(铝、镁、硼)及其氧化物属性见表11-1
2.金属燃烧的分类
根据金属及其氧化物属性特点,可将金属燃烧分类如下:
(1)气相燃烧:对于铝、镁等,氧化物沸点高于金属,表面反应活化能不高故燃烧的主要形式为产生金属蒸汽,形成扩散火焰。
(2)非气相燃烧:对于钨、硼等,沸点高于氧化物,表面反应活化能不太高燃烧类似碳燃烧。
3.决定金属燃烧特点的因素
大量试验表明,决定金属燃烧特点的因素包括以下几点:
(1)推进剂组分组成(金属含量、氧化剂含量、催化剂使用)。
(2)金属与氧化物的热膨胀系数。
(3)金属的熔点及沸点。
(4)金属氧化物的熔点及沸点。
(5)金属在氧化物中的融解特性。
11.2含铝复合推进剂燃烧
11.2.1铝的点火与燃烧
1.燃烧物理过程及现象
如图11-1所示为铝粒子点火燃烧过程。通过实验确定含铝推进剂中铝燃烧过程由以下5步组成。
图11-1铝粒子点火燃烧过程
(1)颗粒着火前的熔合:具有表面氧化膜的原始铝颗粒在接近燃烧表面时铝被熔化,在燃烧表面上,一旦颗粒相互接触,则在氧化膜完全熔化之前,紧挨的原始氧化膜因热应力作用而发生机械破坏,在破坏的地方,颗粒熔合在一起。
(2)着火并形成球形结团:上述固体氧化膜的机械破坏还导致燃面上铝颗粒的着火,在着火瞬间,氧化膜融化,此后形成的结团具有球形状。
(3)多相燃烧:汽化的氧化剂经熔融的氧化膜(它覆盖整个结团)扩散,并与液态铝相互作用,从而使结团温度升高、氧化膜厚度增大。
(4)氧化膜破裂:由于铝的汽化,其蒸汽使致密的液体氧化膜破裂。
(5)蒸汽相燃烧:
1)低压下,氧化膜主要集中在氧化物的一个“疣”上,它占据结团表面的40%~50%,金属从未被氧化物“疣”占据的表面蒸发,气相燃烧位于此表面之上;
2)高压下,整个氧化膜破裂,并形成很小的氧化物颗粒,它们可被铝的蒸汽从结团表面吹走,故整个结团表面进行铝的蒸发,气相燃烧包围整个结团。
2.燃烧数学模型
单金属颗粒在氧化剂氛围中燃烧的实验研究表明,颗粒直径随时间变化关系通常可用如下关系式表示:
\(-\frac{d}{dt}{{D}^{n}}=const\) (n=1.35~1.90) (11-1)
式中,D为颗粒直径;t为时间;n为参数。
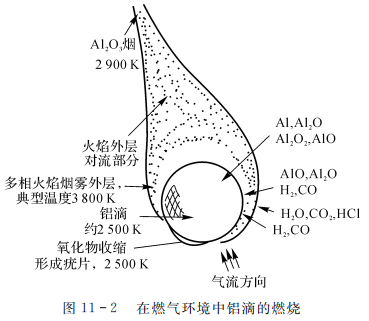
在燃气环境中铝滴的燃烧如图11-2所示。
对于含铝推进剂中铝的燃烧,要考虑含铝推进剂燃烧时铝具体环境因素:
(1)推进剂中铝含量增加,金属发生严重结团现象,进入气流的铝结团尺寸比进入推进剂的原始铝颗粒尺寸大得多;
(2)推进剂中铝含量增加,氧化介质气体(\(C{{O}_{2}}{{H}_{2}}O{{O}_{2}}\)已耗尽)的组成将有所恶化,有效氧含量降低。
因此,必须对颗粒直径随时间变化公式进行修正。
比较有代表意义的铝颗粒直径变化模型为
\(\frac{dD}{dt}=-k{{D}^{1-n}}{{\alpha }^{0.9}}\) (11-2)
式中,D为铝团尺寸;k为系数;t为时间;n为参数;a为氧化性气体摩尔分数之和。
对于铝团来说,其燃烧时间计算模型为
\(t=kD_{0}^{n}/{{\alpha }^{0.9}}\) (11-3)
式中,D为铝颗粒原始尺寸;k为系数;n为参数;为氧化性气体摩尔分数之和。
式(11-2)和式(11-3)都是研究人员从大量实验得到的经验公式,对于不同配方的推进剂,其相关参数都要改变。例如,当k=5.0×10-6,n=1.75,P=1.5,D=150m时,可计算得到t=0.03s。
11.2.2铝的结团
1.结团原因及影响因素
推进剂燃烧时铝颗粒结团是一个极复杂的动力学过程,可具体描述如下:
推进剂燃烧时,黏合剂受热分解产生的中间产物和其溶化物在燃面上形成一个薄薄的液态表面反应层,温度范围675~975K此时,铝(熔点933K,沸点2500K)也被加热并溶化,但是铝表面的氧化物(熔点2323K,沸点3253K)不熔解,仍为固态,将铝包裹住,呈颗粒态。在表面反应层表面张力和黏附力的作用下该铝颗粒滞留在表面反应层内。若铝的尺寸小于表面反应层的厚度并随着它以等于燃速的速度后退时,留在其中的铝粒和其他铝粒相遇,逐渐形成铝的积聚当积聚的铝粒温度升高到铝的熔点时,铝粒的体积膨胀,由于氧化铝的热膨胀系数小于铝的热膨胀系数,因此表面的固态氧化铝膜破裂,液态的铝从裂缝中流出,紧密接触部分的铝连接成块。随着铝积聚的增加,其顶部暴露在高温度的气相区,积聚的铝受热溶化并形成更大的铝块。当气动力大于表面张力和黏附力时,铝结块进入气相区。如图11-3所示为铝的积聚和结团过程。
由此可见,铝结团原因中,如下因素尤其重要:
(1)彼此接触是颗粒通过燃烧波时结团的必要条件;
(2)如果金属熔点低于推进剂燃烧表面温度,则颗粒结团是可能的;
(3)金属的低蒸汽压、金属氧化物的高熔点、属氧化膜的保护性等因素均妨碍颗粒着火,延长颗粒在表面的滞留,从而有利于结团;
(4)金属与金属氧化物因热膨胀系数不同而导致金属氧化膜破裂是颗粒结团的原因。
大量实验表明,推进剂配方参数及发动机工作条件对金属颗粒的结团过程均有影响。我们用结团度来表征结团:
对于含铝复合推进剂,影响因素如下:
(1)推进剂配方参数影响结团因素:
氧化剂AP的粒径\({{D}_{AP}}\):AP粒径增大,结团尺寸增大。
AP的容积分数\({{B}_{AP}}\):AP容积分数减小,结团尺寸增大。
铝的粒径\({{D}_{Al}}\):A粒径减小,结团尺寸增大。
铝的容积分数\({{\beta }_{Al}}\):A容积分数增大,结团尺寸增大。
推进剂燃速r:一般认为,燃速减小,结团尺寸增大。
(2)发动机工作条件影响结团因素:
工作压强:效果同燃速类似,根据不同结团机理,结团尺寸随压强升高可能增大、不变和减小。
横流:横流的存在通常使结团尺寸减小。
2.结团模型(口袋模型)
研究人员通过实验发现推进剂显微结构中铝颗粒聚集在一起,小的铝颗粒充满在较大的氧化剂颗粒的间隙之中。他们根据这些实验结果建立了铝的结团口袋模型。
下面分别介绍含有单模态、双模态、多模态氧化剂的推进剂的结团口袋模型。
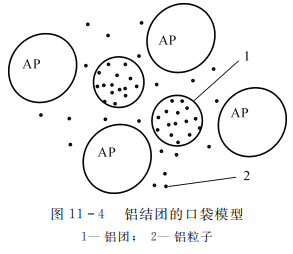
口袋模型,顾名思义,就是像个口袋一样,如图11-4所示为铝结团的口袋模型图。
(1)单模态氧化剂。假设铝颗粒在氧化剂颗粒之间的间隙范围内熔合,从而形成不同尺寸的结团,该尺寸由孔隙量及其中铝含量确定。
根据立体测量学原理,AP颗粒间任意形状的孔隙的容积由当量球的容积确定,该当量球的直径等于AP颗粒表面之间的平均自由距离:
\(l=\frac{4}{{{s}_{AP}}}\frac{1-{{\beta }_{AP}}}{{{\beta }_{AP}}}\) (11-5)
式中\({{s}_{AP}}=\frac{6}{{{D}_{AP}}}\)为氧化剂颗粒的比表面积;为AP占推进剂的容积分数。
结团尺寸的理论值:
说明:①此模型计算的结团尺寸与推进剂燃速及压强无关;②实验表明,在0.1~4mPa压强范围间,理论与实验符合得很好。
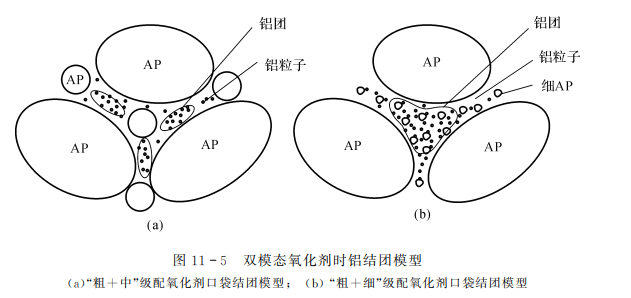
(2)双模态氧化剂。J.K. Sambamurthi等于1984年在单模态氧化剂口袋模型的基础上,利用夹层燃烧模型研究了双模态推进剂中铝的结团(见图11-5)。
双模态推进剂中铝的结团具有如下特点:
1)“粗+中”双级配氧化剂:中粒AP足以使铝颗粒弥散,并对铝着火提供附加的局部扩散小火焰,因而只形成丝状的小结团。
2)“粗+细”双级配氧化剂:口袋由大约等量的AP、铝和黏合剂所充填,且细AP不能建立局部小火焰以点燃铝,因而形成大结团。
3)小火焰仅对高压或大AP颗粒才能建立,故提高压强或加大细AP尺寸时,结团尺寸反而减小。
4)当增加细AP含量时,有利于小火焰建立,从而减少结团。
(3)多模态氧化剂。N.S. Cohen于198年考虑了实际推进剂颗粒尺寸掺混,即多模态的情形,此时,部分AP颗粒直径小于铝颗粒直径,致使口袋的物理图画复杂。
结团由每个口袋内熔融的铝形成,故结团直径正比于口袋内熔融铝质量的三次方根
\({{D}_{ag}}\propto {{(f{{\alpha }_{Al}}{{V}_{p}})}^{\frac{1}{3}}}\) (11-7)
结团分数正比于结团直径:
\({{F}_{ag}}\propto {{D}_{ag}}\propto {{(f{{\alpha }_{Al}}{{V}_{p}})}^{\frac{1}{3}}}\) (11-8)
式中,f为燃面上熔融铝的分数;\({{\alpha }_{Al}}\) 为铝质量分数;\({{V}_{p}}\)为有效口袋容积(定义为最小几何口袋,其内AP将铝包容)。
说明:①若铝不能为最小口袋包容,则它被分配给临近较大的口袋,形成较大结团;②若最小口袋局部火焰温度低(含大量细AP时,局部为富燃环境),铝被分配给临近较大口袋,形成较大结团。
11.2.3铝对推进剂燃速的影响
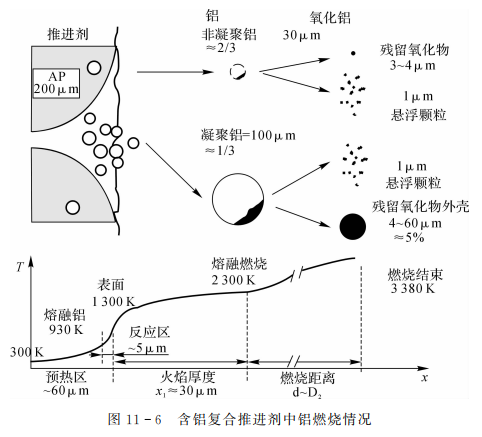
铝粒在燃烧氧化时首先在外表面生成一层氧化铝(Al2O3)的外壳。氧化铝的熔点甚高,约为2300K。由于这一高熔点外壳的保护,壳内的铝不能继续与氧化剂气体反应。要使其中铝粒点燃并完全燃烧,需要更高的温度突破氧化铝的外壳。但AP推进剂燃烧表面的温度只有100K左右,当铝粒从推进剂深处达到燃烧表面时,其温度升高只能使铝本身达到或接近熔化温度,对固态的氧化铝外壳没有多大影响。铝滴在燃烧表面上停留、积聚,互相靠拢,最后形成结团。当然,并不是所有的铝颗粒都参与团聚,部分铝从表面单独逃逸出来直接燃烧。如图11-6所示为含铝复合推进剂中铝燃烧情况。
铝粒或铝团在氧化铝外壳的保护下,离开推进剂的燃烧表面,进入温度更高的燃烧反应区的。随着温度升高,由于氧化铝外壳的膨胀系数小于铝的膨胀系数,外壳被胀裂,铝的熔化液散发出来,就会在氧化剂气体中燃烧。
推进剂中添加金属铝,对于推进剂的燃烧速率有如下影响:
(1)推进剂导热系数增大,有利于提高燃速。
(2)铝表层发生氧化,不利于燃速的提高。
(3)铝燃烧的高发光度,导致辐射换热过程的增强,因而导致燃速增加。
(4)在夹有金属纤维或金属丝的推进剂中,局部的传热可以增大靠近金属丝处的燃烧速率,也相应增加燃烧表面积,有效地增加燃速。
推进剂中加入铝粉,对燃速的提高作用不是很大,但是添加铝有利于增加推进剂理论比冲和密度。
从含铝固体推进剂性能测试结果看,可以做出如下普遍性的概括:
(1)促进铝在表层或近表层燃烧的条件,倾向于提高燃烧速率,并减少对压力的依赖性。
(2)由于直接加入铝,从而使装药更趋于富燃,通常引起燃烧速率的降低,尤其低压下。
(3)如果采用高能量黏合剂,铝对推进剂燃速影响很小。
(4)如果能使燃烧的铝颗粒保留在推进剂表层加速运动,将增大燃速。
11.3含硼富燃料推进剂燃烧
硼以其高的质量热值和容积热值而被认为是固体富燃料推进剂的最佳燃料。硼的质量燃烧热为58280kJ/kg,分别是镁和铝的2.3倍和1.9倍;其体积热值是136.38kJ/cm2,分别是镁和铝的3.09倍和1.66倍。
11.3.1硼点火与燃烧
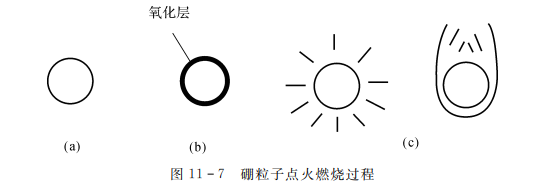
硼点火燃烧过程及现象如图11-7所示。
研究人员发现,当硼粒子在空气中加热到1800~2000K时,它开始发光并持续段时间,如果环境温度足够高,它便进入亮度更强、燃烧更猛烈的第二阶段。一般认为,硼粒子的燃烧过程由两个连续的阶段构成:第一阶段是硼粒子的加热以及它在液态氧化物层的包覆下与氧化性气体的反应,随着氧化层的蒸发和反应生成挥发性产物,氧化物层越来越薄,当它完全挥发(厚度为零)时,第一阶段结束,这一阶段一般认为是点火过程;第二阶段是洁净的硼粒子(无液态氧化层)和周围氧化性气体之间的直接反应,生成最终燃烧产物或过渡性燃烧产物(它进一步氧化生成最终产物),这一阶段是燃烧过程,绝大部分硼是在这一阶段消耗的。
硼粒子在热空气中点火是一个很复杂的过程。硼粒子在周围环境的对流和辐射热作用下被加热,温度升高。当硼粒子温度较低时,其化学反应速率很慢,可以忽略;当温度达到1500K以上时,硼的反应速率很快,反应放热产生自加热作用,并在硼粒子表面产生一层难挥发的玻璃态氧化物。由于氧化层的阻隔,硼和氧必须通过扩散作用才能相互接触并发生化学反应,因此该氧化层的厚度由扩散速率和氧化物的消耗速率决定,一方面通过扩散作用硼与周围环境中的氧发生反应,生成氧化物,产生热量,使氧化层厚度增加,硼粒子温度升高;另一方面通过氧化物的蒸发和与水蒸气的反应使其厚度减小,硼粒子温度降低,当氧化层厚度为零时,点火阶段完成,硼粒子进入燃烧阶段。
1.硼粒子点火机理
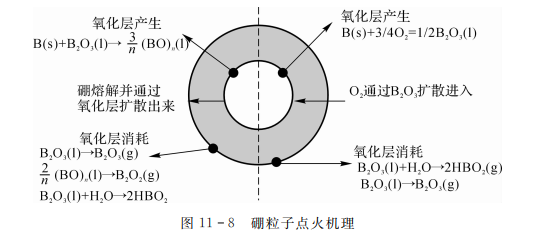
建立硼粒子的点火模型就是以硼的点火机理为基础,确定硼粒子尺寸、氧化层厚度以及硼粒子温度与点火时间之间的关系。在建模过程中,认为硼粒子是不含杂质的球体。如图11-8所示为硼粒子点火机理。
由硼粒子的点火机理可知,其点火时间是由氧化层产生和消耗的速率来决定的,当氧化层的消耗速率大于产生速率时,硼粒子才能点火,消耗速率越大点火时间越短;当氧化层的产生速率大于消耗速率时,氧化层的厚度增加,硼粒子不能点火。
关于氧化层的产生目前存在两种有代表性的观点:
(1)一种是King等人认为,由于浓度梯度,环境中的氧通过液态氧化层扩散到硼与氧化层界面上,并在界面上与硼发生氧化反应产生三氧化二硼(\({{B}_{2}}{{O}_{3}}\)),使氧化层的厚度增加。因此,氧化层产生速率由氧的扩散速率与硼的氧化速率决定,受氧的浓度、压强、氧化层厚度以及硼粒子温度与粒子大小等因素的影响。该化学反应为
式中,下标s,l,g分别表示固态、液态和气态。反应速率为
式中,\({{d}_{p}}\delta {{T}_{p}}{{X}_{{{O}_{2}}}}p\)分别表示硼粒子的直径、氧化层厚度温度以及氧气摩尔分数和环境压强。该速率也即是氧化层的产生速率。
(2)有关氧化层产生的另一种观点是Williams,k.k.kuo等提出的。他们认为,在高温情况下硼在氧化层界面上溶解并与三氧化二硼发生反应,生成聚合物(BO)n,该聚合物在氧化层中由内向外扩散,并在外界面上通过蒸发和化学反应消耗;在低温(一般低于1650K)下硼与氧的反应遵循King的理论。因此,硼溶解生成(BO)n的速率即是氧化层的产生速率,其化学反应为
Williams认为,硼粒子自发点火的一个必要条件是其氧化层厚度必须单调递减,而只有硼的溶解速率等于其消耗速率时,这一条件才能始终满足。因此,(BO)的消耗速率必须等于其产生速率时,硼粒子才能点火。扩散到外表面的部分(BO)与氧发生反应,其反应式为
可得硼的氧化反应式:
K.k.kuo测得硼的氧化反应速率为
其中,\({{P}_{{{O}_{2}}}}{{D}_{BO}}{{n}_{l}}\)分别表示氧气压强\({{\left( BO \right)}_{n}}\) 的扩散系数, \({{T}_{cut}}\)是硼溶解并在氧化层中扩散的最低温度,随的分压力而变,一般情况下可取1650K。
1981年 Safaneev用实验证实硼粒子的点火时间与氧的浓度有关,所测得的点火时间与King公式的理论计算相吻合,使King的观点有了实验基础。 Williams和K.K.Kuo等人则发现:在1050℃时,硼与三氧化二硼反应生成棕色\({{\left( BO \right)}_{n}}\);覆盖在硼粒子外表面的氧化层呈棕色,X射线层析时呈无定型结构。这些现象使他们认为是硼在三氧化二硼中扩散。
氧化层的消耗速率对硼粒子的点火是至关重要的,弄清楚影响氧化层的消耗速率是改善硼粒子点火的基础。关于氧化层的消耗,King与 Williams,k.k.kuo等也有不同的观点(1)King认为,氧化层的消耗是由构成氧化层的三氧化二硼的蒸发及其在外表面与水蒸气的反应,消耗的化学方程式为
\(~{{B}_{2}}{{O}_{3}}\left( l \right)\to ={{B}_{2}}{{O}_{3}}\left( g \right)~\) (11-15)
\(~{{B}_{2}}{{O}_{3}}\left( l \right)+{{H}_{2}}O\left( g \right)=2HB{{O}_{2}}\left( g \right)~\). (11-16)
上式表示\({{B}_{2}}{{O}_{3}}\)的蒸发过程,其速率由两个因索决定:液态\({{B}_{2}}{{O}_{3}}\)的蒸发动力和气态\({{B}_{2}}{{O}_{3}}\)的扩散离开硼粒子的速率。King发现B2O3的蒸发速率可表示为下式:
式中,Nu为努赛尔数。式(11-16)代表\({{B}_{2}}{{O}_{3}}\)和\({{H}_{2}}O\)(水蒸气)的吸热反应,该反应的产物随环境温度不同而异:当气体温度低于140K时,反应产物只有\({{H}_{3}}{{B}_{3}}{{O}_{6}}\),而当气体温度高于2000K时,产物是\(HB{{O}_{2}}\) ;当温度在1400~2000K间,反应产物是很复杂的。由于硼粒子点火的环境温度高于2000K,所以一般取(11-16)式作为\({{B}_{2}}{{O}_{3}}\)和\({{H}_{2}}O\)的反应式。该反应的速率为
式中,\({{X}_{{{H}_{2}}O}}\) 表示水蒸气的摩尔分数。由式(11-7)、式(11-8)可知,氧化层的消耗速率为\({{R}_{E}}+{{R}_{H}}\)。
(2)Williams,k.k.kuo等认为,硼粒子的氧化层由\({{\left( BO \right)}_{n}}+{{B}_{2}}{{O}_{3}}\) 组成,氧化层的消耗由3个独立过程组成:液态三氧化二硼的蒸发,\({{\left( BO \right)}_{n}}\)的蒸发,外表面上\({{\left( BO \right)}_{n}}\)与水蒸气的反应。消耗的化学方程式为
液态三氧化二硼的蒸发化学式同式(11-15),蒸发速率同式(11-17)。式(11-19)表示\({{\left( BO \right)}_{n}}\)的蒸发,K..Kuo测得其速率为
式中\(P_{{{B}_{2}}{{O}_{2}}}^{0},{{D}_{{{B}_{2}}{{O}_{2}},g}},{{r}_{p}}\) 分别表示\({{B}_{2}}{{O}_{2}}\)在硼粒子表面处分压力、扩散系数和硼粒子半径。式(11-20)是与\({{H}_{2}}O\)(水蒸气)反应的化学方程式,其反应速率为
由式(11-12)、式(11-19)、式(11-20)可知(BO)n的消耗速率等于\({{{R}’}_{H}}+{{R}_{{{E}_{BO}}}}+{{{R}’}_{B}}\),从式(11-11)可以得出硼的消耗速率等于\(\frac{2}{3}{{{R}’}_{H}}+\frac{2}{3}{{R}_{{{E}_{BO}}}}+{{{R}’}_{B}}\),此速率即是Williams等人提出的氧化层产生速率。
由以上反应速率可知,无论在哪一种点火理论中,水蒸气的存在总是加速氧化层的消耗, 并且水蒸气的浓度越高,氧化层的消耗速率越大。氧化层的消耗速率随温度的升高而增大,只有当硼粒子的温度高于某一值时,氧化层的消耗速率才会大于其产生速率这一温度即是硼粒子点火的最低温度,实验测得硼在干空气中的最低点火温度为1970K,在湿空气中最低点火温度为1850K。
2硼粒子点火数学模型
为了能比较精确地得到硼粒子点火过程中的一些重要参数,如硼粒子温度、氧化层厚度、半径、点火时间等,建立硼粒子点火的数学模型是必要的。点火过程中硼粒子的参数总是在不断变化的,用微分方程即可动态地描述参数的变化过程。在点火过程中,硼粒子的半径因硼的消耗而不断减小,King认为硼是由氧直接氧化而消耗的其微分方程为
K.k.kuo等认为,硼粒子半径的减小是因为硼不断溶解在氧化层中所致,其微分方程为
氧化物层厚度的变化是由其产生速率和消耗速率决定的,根据King的观点,其微分方程为
由 Williams,k.k.kuo的观点可知,硼的氧化并不影响氧化层厚度的变化,氧化层厚度的微分方程为
点火过程中硼粒子的能量变化是由化学反应热及其与环境的热交换决定的,从King的反应速率中得出能量变化的微分方程为
从Williams的反应速率得出能量变化的微分方程为
其中,\(h({{T}_{g}}-{{T}_{p}}),\sigma {{\varepsilon }_{B}}(T_{amb}^{4}-T_{p}^{4})\) 分别是硼粒子与环境的对流换热、辐射换热。由硼粒子能量变化方程可推导出其温度微分方程,由于硼粒子在点火过程中可能会存在相变过程,因此其温度的微分方程可表示如下:
式中\({{\rho }_{oxide}},{{\rho }_{B}}\) 分别表示硼和氧化物层的密度;\({{C}_{p}}\left( oxide \right)\)表示氧化物层的比热容;\({{Q}_{melt}}\)为硼的熔化热;\({{T}_{melt}}\)为硼的熔点温度;f为液态硼的比例。给定初始条件,应用数学模型即可计算出硼粒子点火过程中的各种参数。由于 Williama,k.k.kuo等人的观点是以高温下硼溶解在其氧化物中这一现象为基础的,因此在温度低于1650K时,由他们的观点导出的方程不能应用。
King和 Williams等为代表提出了两种有代表性的硼粒子在空气中的点火模型:
(1)两种模型的共同点在于,他们都认为水蒸气的存在有利用于硼粒子的点火,硼粒子点火存在一个最低温度,低于该温度硼粒子不能点火。
(2)两种模型的主要差别在于氧化层中的扩散机理不同,King等认为是氧在氧化层中由外向内扩散,而 Williams等则认为是硼在氧化层的内层溶解并向外层扩散。因此,进一步研究硼和氧在液态三氧化二硼中的扩散速率是必要的,弄清楚它们的扩散动力学模型是正确认识硼粒子点火机理的关键。
11.3.2含硼富燃推进剂燃烧模型
对于含硼量30%的含硼富燃推进剂,低压下,相反应是推进剂燃速的控制因素,因此研究含硼富燃推进剂燃烧模型,必须更着重研究凝相区的反应。
含硼富燃推进剂的燃烧过程由两个区构成:凝相反应区和气相燃烧区,在凝相反应区中反应放出的热量,直接被推进剂吸收。低压下,气相燃烧区中释放出的热量只有小部分通过对流和传导等方式反馈到燃面被推进剂吸收。含硼富燃推进剂的燃烧过程具有如下特点:
(1)在燃面以下的凝相反应区中,硼粒子不参与化学反应,其中仍然是AP颗粒和黏合剂基体的反应,这些反应包括:AP颗粒的反应,黏合剂的解聚反应,HTPB的降解、交联和环化,AP分解产生的氧化性气体HTPB或HTPB分解产物之间的反应。
(2)在气相燃烧区中,部分硼粒子在燃烧区的下游发生吸热与放热反应,由于离开燃面的距离很远,这些反应反馈到燃面的热量很小,以忽略不计,因此硼粒子在气相区中的反应并不改变气相区对燃面产生的反馈热结构。
(3)在燃面上方存在一层由硼粒子与碳组成的沉积层,硼在这一层中与AP分解产物进行着大量的界面反应,放出热量因为该沉积层紧贴着燃面,其中的反应热能很快传递到燃面,本文仍然把其中的反应热当作凝相反应热。
(4)和BDP模型有差异的是,由于含硼富燃推进剂中AP含量少,黏合剂含量大,低压下, 当AP分解完成时,黏合剂还不能完全分解,因此会出现HTPB单独进行分解的区域。
(5)含硼富燃推进剂低压下,其气相燃烧波结构存在暗区。
从上述特点可以看到,在含硼富燃推进剂一次燃烧过程中,其凝相反应热与气相反馈热结构与复合推进剂类似,不同的是沉积层中的反应热,因此BDP模型仍然是解释含硼富燃推进剂一次燃烧过程的最好模型,只不过需要在原来的基础上充分考虑到沉积层中的反应热对燃烧过程的影响。
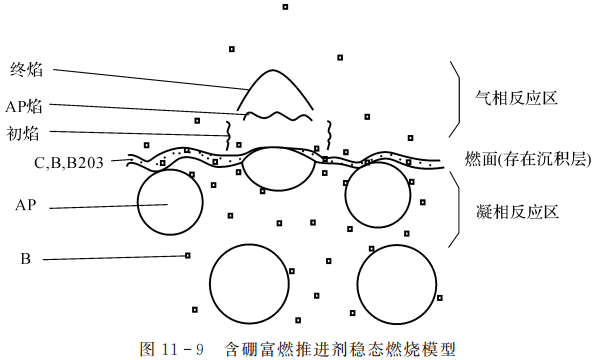
图11-9所示是含硼富燃推进剂燃烧模型示意图。
含硼富燃推进剂稳态燃烧模型具有如下特点:
(1)燃面上存在一层沉积层,其中含有\(C,B,{{B}_{2}}{{O}_{3}}\) ,在沉积层B与AP分解产物进行凝相反应。
(2)和BDP模型类似,存在初焰、AP焰、终焰。
(3)由于含硼富燃推进剂一次燃烧温度不能达到硼的燃点(1850K)因此硼在气相进行反应对燃面的反馈热量可忽略。
习 题
11.1复合推进剂常用金属粉有哪些?
11.2简述金属粉对固体推进剂的性能的影响。
11.3简述含铝推进剂燃烧过程中,铝在燃面上的结团机理。
11.4分析铝粉对推进剂燃速的影响。
11.5分析硼点火燃烧机理。
11.6分析含硼富燃推进剂燃烧模型。
11.7分析铝粉和硼粉在推进剂中的应用差异。